Mgは炎色反応は「なし」と覚えます.
一方でMg粉末やマグネシウムリボンは燃えるときに強い白色光を発することも学びます.

なぜMgは炎中で白色光を発するのでしょうか?
炎色反応とは違うのでしょうか?
今回は,他の炎色反応とは一味違った,Mgの白色光の原理をみていきます.
炎(1):アルカリ金属
炎(2):アルカリ土類金属,銅
炎(3):炎の温度の計算?
炎(4):ガスバーナーの炎の色
炎(5):ロウソクの炎の色
炎(6):Mgの白色光?
炎(7):ロウソクのはじまり
炎(8):近代的なロウソク
炎(9):天然ガスの発見
炎(10):石炭ガス
炎(11):ガス灯の普及
炎(12):石炭から天然ガスへ
[https://omizu-water.hatenablog.com/entry/2023/05/10/180000:title=炎(13):ブンゼンバーナー
炎(14):アセチレンの登場
炎(15):アセチレン炎の利用
1.黒体放射
Mgの白色光は,どんな状態でも生じるわけではありません.Mgの固体を燃やしたときに生じます.Naなどは水溶液を炎中に噴射しても色が変わりますので,その点が通常の炎色反応とは違いますね.
さて,前回も確認したように,熱くなった物体からは黒体放射と呼ばれる過程で光が放出されます.その波長は,材質によらず温度によって決まります.
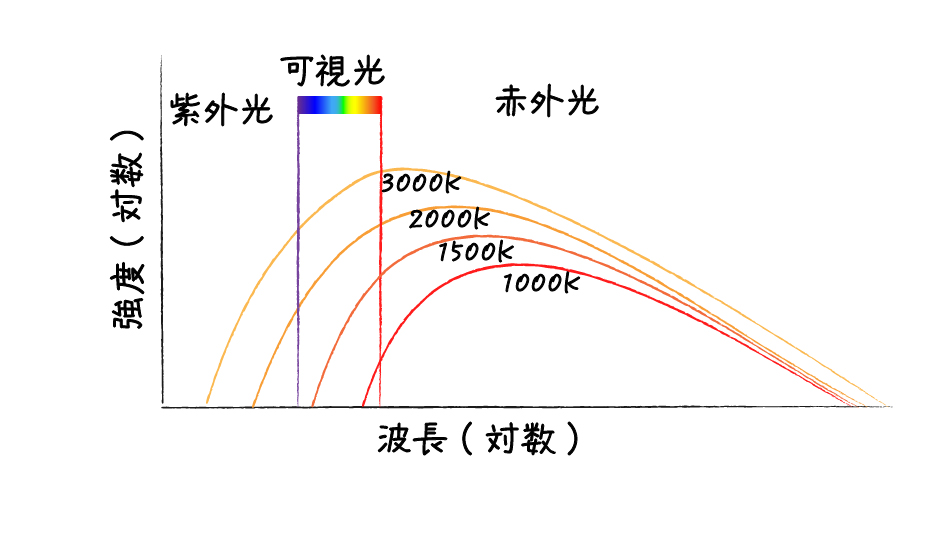
Mg粉末燃焼時の白色光は,純粋に黒体放射だけによると考えると約3600℃(3900K)くらいの色温度になると推定されます.
そんなに熱くなるのでしょうか?
確かにマグネシウムの燃焼で熱は発生しますが,実際にはそこまで熱くならず,2000℃前後,高くても2800℃以下程度のようです.MgOの融点は2800℃ほどですので,炎中でMgOは固体粒子として存在します.
スペクトルから考えると約3600℃(3900K)だけれでも実際は2800℃以下ということは,実際の温度よりも短波長側の光が強いということになります.これは,黒体放射以外のしくみをさらに考慮する必要があることを示しています.
2.ケミルミネッセンス
まず考えられるのはMg原子由来の光ですが,Mg原子もかなり高温では紫外光 (285.2 nm, 3p→3s) を発するのですが,なかなか検出されません.
一方で,MgOからは緑色(480-500 nm)や濃い青色(350-400 nm)の光がケミルミネッセンスと呼ばれる過程で放出されます.化学反応式は以下の通りです.
ケミルミネッセンスでは,このように励起された分子が反応によって直接生成され,光を放出します.放出される光はある程度波長に幅がある,連続光であることが多いです.
熱くなったMgO粒子からの黒体放射に,MgOのケミルミネッセンスが混ざることで,色温度が約3600℃(3900K)くらいの白色の光がみえていると考えられます.
3.散乱
最後にもうひとつ考慮すべき要素として,散乱があります.

炎中のMgO粒子の大きさは約180 nmで,可視光の波長(380-780 nm)とそこまで差がありません.
一般に,を粒子径としたとき,
が1に近いと可視光全体を散乱させ白く輝きます.これをミー散乱と呼び,100-1000 nmくらいの粒子が該当します.雲が白く見えるのはこのためです.
一方で1よりだいぶ小さいと短波長側の光がよく散乱され,青っぽく見えます.これをレイリー散乱と呼び,50 nm以下くらいの粒子がこれに含まれます.空が青く見えるのはこのためですね.
今回のMgO粒子は主にミー散乱がおきます.結果として,黒体放射やケミルミネッセンスで生じた光がMgO粒子によって散乱され,まぶしく輝く白色光になると考えられます.
ちなみに,ロウソクの炎中の炭素粒子は最大で200 nmくらいですので,ミー散乱がおきます.結果として,ロウソクの炎は明るくきれいなオレンジ色に輝くことになります.
omizu-water.hatenablog.com
4.白色光の利用
かつて,こうしたMgの白色光は,カメラのフラッシュなどにも使われました.カメラのフラッシュで使われていた閃光粉は,KNO3が酸化剤としてつかわれていました.化学反応式は以下の通りです.

ちなみに酸化剤としてNaNO3を過剰に混ぜると,ゆっくり反応が進行します.
照明や信号がわりに使われることもあるようです.
こうした白色光は,花火でもよく使われています.
【参考】花火のしくみ(4):フラッシュ,スパーク
また,酸化カルシウム (quicklime) CaOもこうした白色光を発することが知られています.

水素とともに加熱し,そこに酸素ガスを吹き付けるとまばゆい光を放ちます.石灰 limeで光るので,ライムライトとも呼ばれました*1.この現象は1820年代にGoldsworthy Gurney (1793-1875) によって発見されました.

1825年Thomas Drummond (1797-1840) は,Michael Faradayがライムライトを実演していたのを見物し,これを照明につかうことを思いつきました.こうして得られたライムライトは当時使われていたオイルランプの37倍明るかったそうです.
ちょうどこの時期,イギリス軍は1801年に全域を併合したアイルランドの測量を行っていました.当初は日光を鏡で反射させたりオイルランプの光を用いて,これを双眼鏡で確認するという方法がとられていました.しかしこれではなかなか測量は進みませんでした.
そこでDrummondが発明した照明器具を用いたところ,100 km先からでもこの光が確認できるということで測量が大きく進みました.大活躍ですね.

また,Drummondのライムライトは劇場でも大変活躍しました.当時の照明器具といえばガス灯やアーク灯でしたが,ガス灯は煙がすごく,アーク灯*2は強すぎるという問題がありました.一方でライムライトは煙もでず,光もいい感じの強さで,登場人物を効果的に照らすことができました.スポットライトの誕生です.

1837年,ロイヤルオペラハウスでライムライトがステージライトとして使われました.当時,水素ガスや酸素ガスはそのまんまでは売っていなかったので,化学反応を用いて用意する必要がありました.そこで,水素ガスは希硫酸を亜鉛と反応させて用意し,
酸素ガスは塩素酸カリウム,硝酸ナトリウムなどを加熱して用意しました.この頃の酸素ガスのメインの用途は,実はライムライトだったそうです.
これらははじめゴム袋に溜められ,木の板などではさんで圧力をかけて保存していたようです.当然やぶれたりすることもあり,大変危険でした.
電球が普及した現在ではライムライト自体は使われていませんが,名声を表す単語として今でも残っています.

5.まとめ
Mgの白色光は炎色反応とはいいませんが,意外と奥が深いということがわかったと思います.
今回は省略してしまいましたが,レイリー散乱的な散乱による波長シフトも考慮することがあるようです.
このあたりはAl粉末の白色光でよく研究されているようです.
次は,ロウソクの歴史を見てみましょう.
問題
Q.雨雲が灰色にみえるのはなぜだろう?
A.雨雲によって光が吸収され,目に届く光が減るから.
実際,MgOやAl2O3粒子などについても散乱の他に吸収の波長依存性なども考慮する必要があります.
参考文献
"Flame Spectroscopy" Mavrodineanu, R. and Boiteux, H. (1965).
"The Spectroscopy of Flames" Gaydon, A.G. (1974).
"Flames: Their Structure Radiation and Temperature" Gaydon, A.G., Wolfhard, H.G. (1979).
"The Anomalous Brightness of Magnesium-Air Flames" Newman, R.N., Payne, J.F.B., Combustion and Flame, 68, 31-41 (1987)
"Candoluminescence and radical-excited luminescence" H.F. Ivey, Journal of Luminescence 8, 271-307 (1974).
"History of Industrial Gas" E. Almpvist Springer (2002).